Introduction à l’épidémiologie des radiations : étude du risque de cancer
Publié en ligne le 15 mai 2026 - Ondes électromagnétiques -
L’épidémiologie des radiations est l’étude des conséquences de l’exposition des populations humaines aux radiations ionisantes. La conséquence principale est une augmentation du risque de cancer, et nous nous limiterons à l’étude de ce risque et plus précisément du risque de cancer solide, c’est-à-dire excluant les cancers hématologiques : leucémies, lymphomes, etc. Dans toute la suite du texte, pour simplifier, on utilisera le terme « cancer » pour les cancers solides.
Le risque dépend de la dose d’irradiation, dose qui se mesure en millisievert (mSv). Une dose de moins de 10 mSv est considérée comme très faible, une dose d’au moins 10 mSv mais inférieure à 100 mSv est une faible dose, une dose d’au moins 100 mSv mais inférieure à 1 000 mSv est une dose modérée et une dose de 1 000 mSv ou plus est une forte dose (pour une explication de l’unité de mesure – le millisievert, ou mSv – voir l’introduction du dossier).
Chacun d’entre nous est exposé à l’irradiation naturelle due au gaz radon et autres rayonnements d’origine tellurique et cosmique (accrus lors des voyages en avion), aux aliments, au tabac, aux examens diagnostiques radiologiques et à certains traitements médicaux. On estime qu’en France, l’exposition moyenne de la population est de 4,5 mSv par an [1], mais cette exposition est très variable. Par exemple, dans un territoire à forte concentration en radon, la dose moyenne peut dépasser 10 mSv par an (voir [1] pour un calculateur de dose). Les expositions annuelles se cumulent ; ainsi une moyenne de 3 mSv par an donnera au bout de 40 ans une dose cumulée de 120 mSv.
Les enquêtes
De nombreuses enquêtes épidémiologiques ont étudié les risques de cancer en fonction de la dose supplémentaire provenant d’une source identifiée. On a ainsi étudié les survivants des bombes atomiques d’Hiroshima et Nagasaki, les mineurs de fond exposés au radon, les travailleurs de l’industrie nucléaire, les patients ayant subi des scanners, etc. Nous présentons les résultats d’une sélection de ces enquêtes.
Pour étudier le risque de cancer en fonction de la dose, il faut reconstituer l’historique de l’exposition cumulée de chaque personne. Par exemple, pour un survivant des bombardements, l’exposition due au bombardement est égale à 0 avant le bombardement et à une valeur constante ensuite, qui dépend de sa position au moment de l’explosion. Pour un travailleur, l’historique commence à l’embauche, moment où son exposition professionnelle cumulée est égale à 0 à un âge a0. Cette exposition professionnelle cumulée évolue ensuite en fonction de son âge selon une fonction qui peut rester constante ou augmenter, mais ne peut pas diminuer.
On cherche à estimer le risque de cancer en fonction de l’exposition cumulée, qui est découpée en intervalles définis. Dans l’enquête Inworks, les seuils de dose étaient 10, 25, 50, 100, 150, 200, 300, 400, et 500 mSv. Pour estimer le risque de cancer pour une catégorie de dose, par exemple 100 à 149 mSv, on divise le nombre de cancers diagnostiqués chez des personnes dont la dose cumulée est entre 100 et 149 mSv au moment du diagnostic par la somme des durées de suivi de la population qui a une exposition cumulée entre 100 et 149 mSv. Un travailleur est à risque de cancer avec une exposition cumulée de 100 à 149 mSv tant que son exposition cumulée reste dans cet intervalle de dose. Le suivi d’un même travailleur peut ainsi contribuer à l’estimation des risques dans plusieurs catégories de dose, au fur et à mesure que son exposition cumulée évolue.
En réalité, ces calculs sont faits séparément, notamment par sexe et par classe d’âge, mais rentrer dans ces détails dépasserait les limites de cet encadré.
Survivants des bombardements d’Hiroshima et de Nagasaki
Le 6 août 1945, une bombe atomique fut larguée sur la ville d’Hiroshima, suivie trois jours plus tard par une bombe sur Nagasaki. La population totale était d’environ 600 000 personnes, et 200 000 décès à court terme ont été causés par le souffle et la chaleur de l’explosion. À partir de 1950, un suivi épidémiologique des personnes irradiées a été mis en place sous le nom de « Life Span Study (LSS) ». Il se poursuit encore aujourd’hui.
Les études portent sur près de 87 000 survivants pour lesquels une dose d’irradiation a pu être estimée. Cette dose varie de 0 à environ 4 000 mSv : 79 % des personnes ont reçu moins de 100 mSv, 18 % entre 100 mSv et 1 000 mSv, et 3 % 1 000 mSv ou plus. La dose moyenne est de 116 mSv [2].
Le risque relatif de cancer (rapport des risques dans la population exposée et dans la population témoin, populations suivies jusqu’en 2003) augmente en fonction de la dose (voir encadré ci-dessous). Si les survivants des bombardements avaient été exposés au même risque de décès par cancer que la population japonaise non exposée, 10 402 décès auraient été observés au lieu des 10 929 (527 décès supplémentaires), le risque a donc été augmenté de 5 % (527/10 402).
Risque relatif de décès pour l’ensemble des cancers en fonction de la dose de rayonnements ionisants due au bombardement.
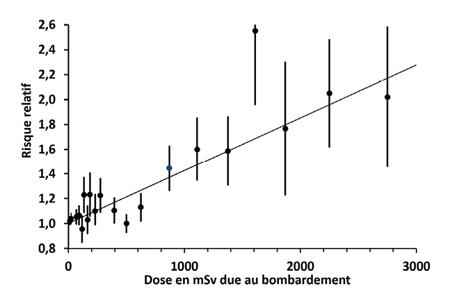
Les points représentent le risque relatif dans les différentes classes de dose additionnelle et les traits verticaux leur précision (intervalle de confiance à 95 %). La pente de la droite est le résultat d’un calcul, le principe étant de minimiser la distance entre la droite et les observations, en donnant plus de poids aux points estimés avec plus de précision. Pour une dose additionnelle de 3 000 mSv, 15 fois plus grande que la dose hors bombardement accumulée en 50 ans à raison d’une exposition annuelle de 4 mSv, le risque de cancer est à peu près doublé. Le risque augmente de 42 % pour une exposition de 1 000 mSv.
Source Ozasa K et al., “Studies of the mortality of atomic bomb survivors, report 14, 1950–2003 : an overview of cancer and noncancer diseases”, Radiation Research, 2012, 177 :229-43.

Travailleurs de l’industrie nucléaire
Contrairement aux survivants des bombardements, les travailleurs de l’industrie nucléaire ont une exposition aux rayonnements ionisants due à leur travail qui est étalée dans le temps. Leur dose professionnelle cumulée est en moyenne de 18 mSv mais peut dépasser 1 000 mSv chez quelques travailleurs. Cette exposition est surveillée par le port d’un dosimètre dont les mesures sont archivées. Cela a permis une série d’études dans ces populations, dont la plus récente est l’étude Inworks [3] qui a inclus près de 310 000 travailleurs suivis en moyenne 35 ans. Elle présente une mise à jour des données sur les travailleurs de trois pays (France, Royaume-Uni, États-Unis) qui faisaient déjà partie de l’étude antérieure sur les travailleurs de 15 pays [4].
Un peu plus de 28 000 cancers solides ont été observés et le risque relatif de ces cancers (voir encadré ci-dessous pour la façon de le calculer) a été étudié en fonction de la dose. Les estimations du risque relatif dans les différentes classes de dose avec leurs précisions sont présentées dans l’encadré ; la précision est meilleure pour les doses les plus faibles car davantage de travailleurs y ont été exposés.
Dans l’ensemble, le risque relatif augmente avec la dose et un modèle linéaire résume les données d’une façon adéquate : le risque augmente de 4,2 % pour une dose supplémentaire de 100 mSv.
Risque relatif de décès par cancer en fonction de la dose cumulée reçue jusqu’à 10 ans avant le cancer.
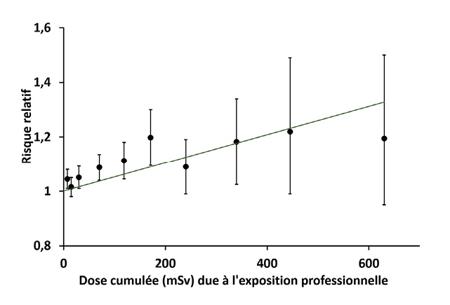
L’analyse est ajustée sur le pays, l’âge, le sexe, l’année de naissance, le statut socioéconomique, la durée de l’emploi, et la surveillance ou non d’une exposition aux neutrons (voir figure 1).
Source Richardson DB et al., “Cancer mortality after low dose exposure to ionising radiation in workers in France, the United Kingdom, and the United States (INWORKS) : cohort study”, The British Medical Journal, 2023, 382 :e074520.)
Personnes ayant eu des scanners dans l’enfance
Plusieurs enquêtes ont suivi des populations ayant eu des scanners dans l’enfance. Une enquête réalisée dans neuf pays d’Europe de l’Ouest a inclus près d’un million de personnes ayant eu au moins un scanner avant l’âge de 22 ans pour une raison médicale. L’étude du risque de tumeur cérébrale a porté sur près de 660 000 personnes étudiées en excluant une période de cinq ans après leur premier scanner, et suivies pendant une durée médiane de 5,6 ans. La moitié des patients avaient reçu une dose au cerveau cumulée jusqu’à 5 ans avant le diagnostic dépassant 47 mSv, avec un maximum de 4 000 mSv. Un total de 165 tumeurs céré brales malignes ont été observées, à comparer aux 99 tumeurs attendues dans cette population en l’absence de scanner. Ces 66 tumeurs en plus correspondent à 0,01 % de la population exposée.
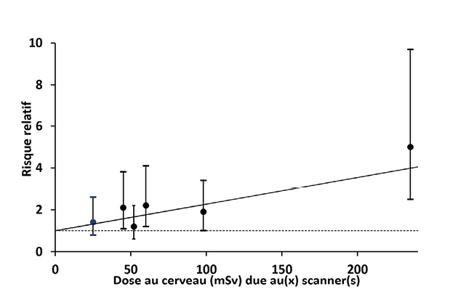
Les estimations du risque relatif en fonction de la dose au cerveau avec leur intervalle de confiance à 95 % sont présentées en encadré ci-après. Dans l’ensemble, le risque relatif augmente avec la dose.
La droite représente le résultat du modèle linéaire. Le risque relatif est égal à 2,27 pour une dose additionnelle au cerveau de 100 mSv reçue plus de cinq ans avant le diagnostic de tumeur cérébrale. Pour 10 000 personnes ayant subi un seul scanner qui a délivré une dose d’environ 38 mSv, on attend une tumeur cérébrale maligne en plus dans une période de 5 à 15 ans après le scanner [5]. Mais ces scanners ont certainement contribué à éviter un très grand nombre de problèmes beaucoup plus immédiats.

Risque de tumeur cérébrale après scanner en fonction de la dose d’irradiation, dans une population de 0 à 22 ans (voir figure 1).
Source Hauptmann M et al., “Brain cancer after radiation exposure from CT examinations of children and young adults : results from the EPI-CT cohort study” The Lancet Oncology, 2023, , The Lancet Oncology, 2023, 24 :45-53.
Exposition au radon
En France, les habitants de certaines parties du Massif central et de la Bretagne sont naturellement exposés au radon, gaz radioactif qui émane du sol et pénètre dans les bâtiments. Les doses mesurées en becquerel par m3 (Bq/m3) sont très variables d’un bâtiment à l’autre (le becquerel mesure le nombre de désintégrations par seconde – voir introduction du dossier). Les effets du radon ont été étudiés chez les mineurs de fond, dont les expositions sont, et surtout étaient dans le passé, particulièrement fortes, et dans les populations exposées dans leur habitation. Certaines des premières études sur les effets de l’exposition au radon dans les habitations ont étudié le lien entre la fréquence des cancers du poumon et le niveau moyen de radon dans différentes zones géographiques ; mais ces études dites écologiques ne pouvaient pas prendre en compte les facteurs de confusion potentiels (facteurs liés à la fois à l’exposition au radon et au risque étudié), notamment le tabagisme, ainsi que le fait que la concentration de radon varie considérablement d’une maison à l’autre dans une même zone géographique (selon le type de sol, les fondations, les éventuelle fissures, l’étanchéité, la ventilation, etc.).
La plupart des enquêtes épidémiologiques sur le radon domestique et le cancer du poumon sont des enquêtes cas-témoins dans lesquelles on a comparé les expositions au tabac et au radon de patients atteints d’un cancer du poumon et de témoins sans cancer du poumon.

La synthèse de 13 enquêtes cas-témoins réalisées dans neuf pays d’Europe rapporte une augmentation du risque relatif de 16 % par 100 Bq/m3 d’augmentation du radon dans les logements successifs de la personne concernée. Ce type d’enquête est ici très fiable parce que l’exposition a été mesurée dans les logements au lieu de dépendre du résultat d’un questionnement des participants. L’exposition moyenne des témoins de la partie française de cette enquête était de 120 Bq/m3 et cette moyenne peut dépasser 300 Bq/m3 dans certaines communes (voir encadré ci-après) [6].
Dans ces enquêtes, les personnes étaient aussi interrogées sur leur consommation de tabac, ce qui a permis l’étude des effets conjoints du tabac et du radon. La mortalité par cancer du poumon cumulée jusqu’à l’âge de 75 ans augmente en fonction de la dose de radon séparément chez les fumeurs de cigarette et chez les personnes n’ayant jamais fumé, et les effets du tabac et du radon sont multiplicatifs. La consommation de tabac multiplie le risque de cancer du poumon cumulé jusqu’à 75 ans par 24, le radon par 2,2, et l’association des deux par 53. L’effet de la dose est donc beaucoup plus important chez les fumeurs.
Source Darby S et al., “Radon in homes and risk of lung cancer : collaborative analysis of individual data from 13 European case-control studies”, The British Medical Journal, 2005, 330 :223.

Rubens a souvent représenté le nu féminin, et certains médecins et radiologues estiment aujourd’hui qu’il n’hésitait pas à représenter sans fard la réalité anatomique de ses observations : ici, la Grâce de droite semble présenter une tumeur cancéreuse caractéristique sur son sein gauche.
Conséquences de ces enquêtes pour la radioprotection
Les résultats des études présentés ici, comme ceux des autres études du risque de cancer (hors leucémie), sont compatibles avec une augmentation linéaire du risque en fonction de la dose additionnelle de radiation.
Les modèles permettent d’extrapoler les résultats des enquêtes pour les appliquer à d’autres populations. Ils servent aussi à argumenter les limites réglementaires pour les expositions des travailleurs.
On a ainsi pu estimer que les effets de l’accident de Tchernobyl sur la population française ont été trop faibles pour être détectables [7].
Une étude a récemment estimé le nombre des cancers attendus dans l’avenir qui seront les conséquences des 93 millions de scanners effectués en 2023 sur 61,5 millions de patients (dont 4,2 % d’enfants) aux États-Unis [8]. Les doses de rayonnement délivrées par les différents types de scanner aux organes cibles ont été estimées en fonction de l’âge, du sexe et du type de scanner, et les risques des différents types de cancer en fonction de la dose de rayonnement aux différents organes ont été estimés en utilisant les modèles du National Research Council’s Biological Effects of Ionizing Radiation VII [9]. Cette étude montre que, compte tenu de l’utilisation actuelle et des doses d’irradiation, les scanners faits en 2023 devraient entraîner environ 103 000 cancers futurs au cours de la vie des patients exposés, dont 10 000 dus aux scanners chez les enfants et 93 000 aux scanners chez les adultes. On s’attend donc à observer 1,1 cancers (103 000/93 000) pour 1 000 scanners. Si le nombre de cancers et l’usage des scanners ainsi que les doses qu’ils délivrent restent stables aux États-Unis dans le futur, les scanners pourraient être responsables d’environ 5 % des cancers diagnostiqués chaque année.
Discussion
Les enquêtes épidémiologiques ont été très bien faites mais les estimations de risque qu’on en tire sont contestées par certains experts qui pensent qu’il n’est pas légitime d’extrapoler un risque aux faibles doses à partir des données observées. Il s’agit d’un malentendu, car les enquêtes épidémiologiques ne comparent pas une population exposée aux radiations à une population sans aucune exposition aux radiations, une telle population n’existant pas. Elles étudient les risques chez des personnes qui sont exposées à une dose variable (professionnelle, médicale diagnostique ou environnementale comme le radon) qui s’ajoute aux radiations habituelles. Les risques relatifs calculés sont les rapports entre le risque pour une dose additionnelle donnée et le risque sans dose additionnelle.
« Tous les modèles sont faux mais certains sont utiles » aurait dit le statisticien américain George Box. Si vous n’êtes pas convaincus par les modèles, il suffit de supprimer mentalement dans les encadrés les droites qui essaient de résumer les tendances pour ne conserver que les résultats des observations : estimations ponctuelles dans les différentes classes de dose avec leur intervalle de confiance. Mais ceci empêchera toute estimation des conséquences des expositions dont les effets n’ont pas été mesurés directement.
Les risques associés à l’exposition aux rayonnements ionisants ont fait l’objet de très nombreux travaux impliquant des centaines de chercheurs. Et la surveillance des conséquences des expositions médicales et des expositions professionnelles va certainement continuer.
Conclusion
Le risque de cancer associé à une exposition aux radiations ionisantes dépend de la dose, et toute exposition à une dose supplémentaire augmente le risque. Cette augmentation du risque est approximativement linéaire. Une dose supplémentaire cumulée de 100 mSv augmente le risque d’un peu moins de 5 %. Cette valeur de 100 mSv est l’équivalent d’une exposition à la radioactivité naturelle moyenne en France sur environ 20 ans.
Les radiations ionisantes font peur, mais nous sommes tous exposés à une irradiation naturelle en partie inévitable. Ainsi, une grande partie de la population n’est pas prête à renoncer aux voyages en avion. Et les rayonnements ionisants ne sont pas un cancérogène très efficace. Le suivi des populations d’Hiroshima et Nagasaki qui étaient en vie en 1950 montre une augmentation du risque de cancer de 5 % – ce qui n’est pas considérable, et correspond à une multiplication du risque par 1,05. Pour mémoire l’association de la consommation associée d’au moins 4 grammes de tabac et de 30 grammes d’alcool pur par jour multiplie les risques de cancer du pharynx et du larynx par 35.
1 | Autorité de sûreté nucléaire et de radioprotection, « L’exposition de la population », septembre 2016. Sur irsn.fr
2 | Ozasa K et al., “Studies of the mortality of atomic bomb survivors, report 14, 1950–2003 : an overview of cancer and noncancer diseases”, Radiation Research, 2012, 177 :229-43.
3 | Richardson DB et al., “Cancer mortality after low dose exposure to ionising radiation in workers in France, the United Kingdom, and the United States (INWORKS) : cohort study”, The British Medical Journal, 2023, 382 :e074520.
4 | Cardis E et al., “The 15-country collaborative study of cancer risk among radiation workers in the nuclear industry : estimates of radiation-related cancer risks”, Radiation Research, 2007, 167 :396-416.
5 | Hauptmann M et al., “Brain cancer after radiation exposure from CT examinations of children and young adults : results from the EPI-CT cohort study”, The Lancet Oncology, 2023, 24 :45-53.
6 | Darby S et al., “Radon in homes and risk of lung cancer : collaborative analysis of individual data from 13 European casecontrol studies”, The British Medical Journal, 2005, 330 :223.
7 | Cardis E et al., “Estimates of the cancer burden in Europe from radioactive fallout from the Chernobyl accident”, International Journal of Cancer, 2006, 119 :1224-35.
8 | Smith-Bindman R et al.,“Projected lifetime cancer risks from current computed tomography imaging”, JAMA Internal Medicine, 2025, 185 :710-9.
9 | National Research Council, Health Risks from Exposure to Low Levels of Ionizing Radiation : BEIR VII Phase 2, National Academies Press, 2006.
Publié dans le n° 355 de la revue
Partager cet article
L'auteur
Catherine Hill

Catherine Hill est épidémiologiste et biostatisticienne, spécialiste de l’étude de la fréquence et des causes du (…)
Plus d'informationsOndes électromagnétiques

Ondes santé et justice : Menons l’enquête
Le 25 janvier 2025
Effets sanitaires de la 5G : des expertises et une polémique sans fin
Le 24 octobre 2020















![[Lyon - Mardi 23 septembre 2025 à 20H30] Ondes et santé : quoi de nouveau avec la 5G ?](local/cache-gd2/f7/9a71838634b9a9e32ff175d195856f.png?1753449505)









